Mondo
Via libera dell’Europa al primo vaccino anti-malaria
L'Agenzia europea dei farmaci (Ema) ha dato il nulla osta all'uso del Mosquirix al di fuori dell'Unione europea, nei Paesi in cui la malaria è endemica, per l'immunizzazione dei bimbi da 6 settimane a 17 mesi
di Redazione
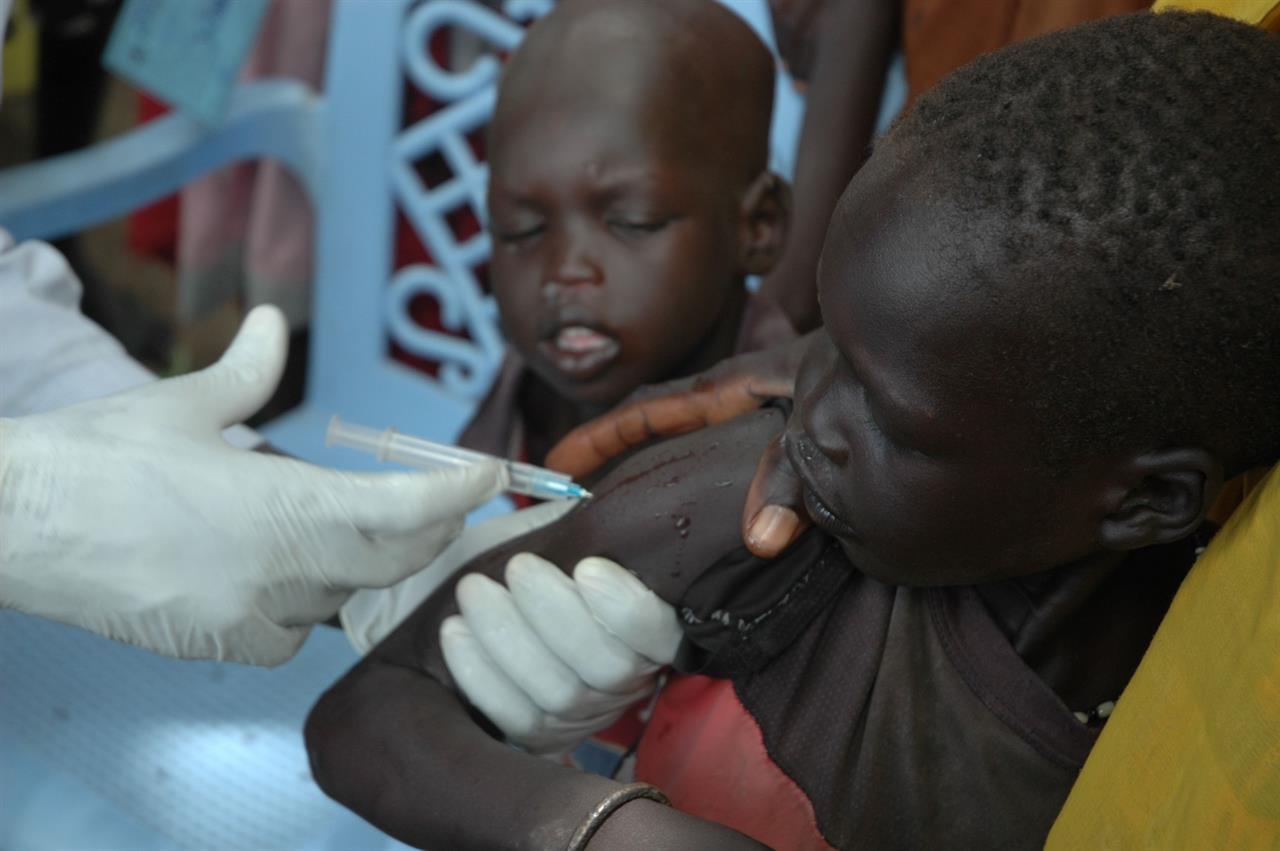
Via libera dell’Agenzia europea dei farmaci (Ema) al primo vaccino al mondo contro la malaria. Una notizia accolta dai festeggiamenti degli scienziati in Africa: il comitato di esperti (Chmp) dell’Ema ha espresso parere positivo per l’uso di Mosquirix al di fuori dell’Unione europea, nei Paesi in cui la malaria è endemica, per l’immunizzazione dei bimbi da 6 settimane a 17 mesi. È efficace contro il parassita che causa la malattia, ma anche contro l’epatite B.
Alla base del vaccino ci sono 30 anni di ricerca, illustrati nelle circa 230 mila pagine di dati sottoposte all’Ema. Nel 2001, l’azienda britannica Gsk e Path Malaria Vaccine Initiative, con un primo finanziamento ricevuto dalla Bill & Melinda Gates Foundation, hanno creato una partnership pubblico-privata per lo sviluppo di un vaccino contro la malaria. Path ha investito negli anni oltre 200 milioni di dollari, per lo più arrivati dai coniugi Gates. L’investimento di Gsk è stato di più di 356 milioni di dollari, a cui dovranno aggiungersi altri 200-250 milioni per completare lo sviluppo.
Sir Andrew Witty, amministratore delegato di Gsk, ha spiegato che l’approvazione «rappresenta un altro importante passo verso la possibilità di mettere il vaccino a disposizione dei bambini. Sebbene non sia una risposta completa alla malaria, il suo utilizzo abbinato alle contromisure già in uso, come reti per i letti e insetticidi, contribuirà in modo significativo a controllare l’impatto della malattia nei Paesi africani più colpiti».
L’ok europeo dovrà ora essere seguito dall’approvazione dell’Organizzazione mondiale della sanità, che potrebbe pronunciarsi entro la fine dell’anno, e poi dai governi dei singoli Stati africani, che dovranno definire il programma di vaccinazioni. Circa 600 mila persone l’anno muoiono di malaria, la maggior parte nell’Africa sub-sahariana.
Il vaccino è stato sperimentato in 7 paesi africani (Burkina Faso, Gabon, Ghana, Kenya, Malawi, Mozambico e Tanzania), i dati non sono brillantissimi: si è mostrato efficace nel prevenire la malaria nel 56% dei bimbi fra 7-17 mesi e nel 31% dei piccoli di 6-12 settimane. L’efficacia diminuisce dopo un anno, il profilo di sicurezza è accettabile.
È «il principale risultato raggiunto per lo sviluppo di un vaccino contro la malaria, ed un passo avanti verso la decisione delle sue modalità di utilizzo». L’Organizzazione mondiale della sanità accoglie positivamente l’ok dell’Agenzia europea all’uso del siero al di fuori dell’Europa. L’Oms ci tiene contemporaneamente a precisare che il vaccino «non è stato ancora autorizzato in alcun Paese in cui la malaria è endemica. Riteniamo che questo non possa accadere prima del 2017. La valutazione dell’Ema non è una raccomandazione all’utilizzo» del prodotto. L’Oms emanerà le sue raccomandazioni entro novembre di quest’anno. E’ necessario, infine, che i finanziamenti al vaccino per completare lo sviluppo non distolgano risorse da destinare all’uso di zanzariere, farmaci efficaci e test rapidi per la diagnosi della malaria.
Cosa fa VITA?
Da 30 anni VITA è la testata di riferimento dell’innovazione sociale, dell’attivismo civico e del Terzo settore. Siamo un’impresa sociale senza scopo di lucro: raccontiamo storie, promuoviamo campagne, interpelliamo le imprese, la politica e le istituzioni per promuovere i valori dell’interesse generale e del bene comune. Se riusciamo a farlo è grazie a chi decide di sostenerci.
